友情提示
本站部分转载文章,皆来自互联网,仅供参考及分享,并不用于任何商业用途;版权归原作者所有,如涉及作品内容、版权和其他问题,请与本网联系,我们将在第一时间删除内容!
联系邮箱:1042463605@qq.com
国家药典委:人用疫苗总论等6个标准公示
122
0
相关文章
近七日浏览最多
最新文章
5月13日,国家药典委官网发布了6个标准公示,分别为人用疫苗总论国家药品标准、23价肺炎球菌多糖疫苗国家药品标准、注射用人干扰素α1b等七个品种国家标准、碘帕醇国家药品标准、安立生坦国家药品标准和安立生坦片国家药品标准。除了23价肺炎球菌多糖疫苗国家药品标准和人用疫苗总论国家药品标准公示期为3个月,其余同为2个月。

其中,人用疫苗总论标准中7.5.2检测项下增订“因疫苗本身质量属性不适合进行异常毒性检查的,在提供充分依据并经过评估的基础上,经批准可不设立该项检查”。
23价肺炎球菌多糖疫苗国家药品标准中,沉淀粗糖项下将“或按另行批准的工艺沉淀粗糖”修订为“或按另行批准的工艺执行”;去除蛋白项下将“采用冷酚法或经批准的方法去除蛋白质”修订为“采用冷酚法或经批准的方法去除蛋白质;或按另行批准的工艺执行”;去除核酸项下将“采用乙醇沉淀法或经批准的方法去除核酸”修订为“采用乙醇沉淀法或经批准的方法去除核酸;或按另行批准的工艺执行”。
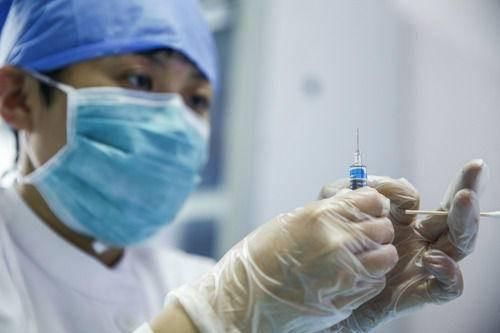
2020年11月25日,工作人员在北京一社区卫生服务中心内为市民接种流感疫苗。新华社记者 张玉薇 摄
友情提示
本站部分转载文章,皆来自互联网,仅供参考及分享,并不用于任何商业用途;版权归原作者所有,如涉及作品内容、版权和其他问题,请与本网联系,我们将在第一时间删除内容!
联系邮箱:1042463605@qq.com